|
|
|
|---|---|
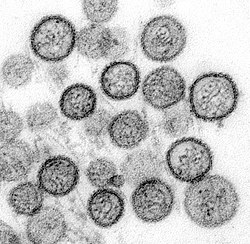 한타바이러스의 한부류인 신 놈브레 바이러스 |
|
| 생물 분류ℹ️ | |
| 과: | Bunyaviridae |
| 속: | Hantavirus |
| 종: | Andes virus (ANDV) Bayou virus (BAYV) |
한타바이러스(영어: Orthohantavirus)는 인간에게 질병을 일으키는 모든 한타바이러스(한타바이러스과, Hantaviridae)를 포함하는 바이러스의 한 속이다. 이하 한타바이러스로 칭하는 오르토한타바이러스는 주로 설치류에서 자연적으로 발견된다. 일반적으로 각 한타바이러스는 하나의 설치류 종에 의해 매개되며, 한타바이러스를 매개하는 각 설치류는 하나의 한타바이러스 종을 매개한다. 자연 숙주 내에서 한타바이러스는 대개 무증상의 지속적인 감염을 일으킨다. 그러나 인간에게 한타바이러스는 두 가지 질병, 즉 신증후출혈열(HFRS)과 한타바이러스 폐증후군(HPS)을 일으킨다. HFRS는 주로 아프리카, 아시아, 유럽에 분포하는 이른바 구대륙 한타바이러스에 의해 발생하며, HPS는 주로 아메리카 대륙에 분포하는 신대륙 한타바이러스에 의해 발생한다.
한타바이러스는 주로 설치류의 배설물이 포함된 에어로졸과 비말을 통해 전파되며, 오염된 음식, 물림, 할큄 등을 통해서도 전파될 수 있다. 남아메리카에서 발견되는 안데스 바이러스(Andes virus)는 접촉자 간의 제한적인 사람 간 전파가 문서화된 현재 알려진 유일한 한타바이러스이다.[1] 강수량, 온도, 습도와 같은 환경적 요인이 전파에 영향을 미친다. HFRS는 신장 비대, 소변 내 과다한 단백질(단백뇨), 소변 내 혈액(혈뇨)을 동반하는 신장 질환이 특징이다. HFRS의 치명률은 바이러스에 따라 1% 미만에서 15%까지 다양하다. 유행성 신병증(nephropathia epidemica)이라고 불리는 경증 형태의 HFRS는 주로 푸말라 바이러스(Puumala virus)와 도브라바-베오그라드 바이러스(Dobrava-Belgrade virus)에 의해 발생한다. HPS의 경우 초기 증상으로 발열, 두통, 근육통 등 독감과 유사한 증상이 나타나며, 이후 갑작스러운 호흡 부전이 뒤따른다. HPS는 치명률이 30~60%로 HFRS보다 높다. HFRS와 HPS 모두 질병은 혈관 투과성 증가, 혈소판 수 감소, 면역 체계의 과잉 반응의 결과로 발생한다.
한타바이러스 유전체는 각각 하나의 단백질을 암호화하는 세 개의 단일 가닥 음성 방향 RNA 분절로 구성된다: RNA 의존성 RNA 중합효소(RdRp), 스파이크 당단백질 전구체, 그리고 N 단백질이다. 분절들은 N 단백질에 둘러싸여 리보핵단백질(RNP) 복합체를 형성하며, 각 복합체에는 RdRp 사본이 부착되어 있다. RNP 복합체는 표면에서 뻗어 나온 스파이크 단백질을 지닌 지질 포막(lipid envelope)으로 둘러싸여 있다. 복제는 스파이크가 세포 표면에 부착될 때 시작된다. 세포 내로 진입한 후 포막은 엔도솜 및 리소좀과 융합하여 RNP를 세포질로 방출한다. 그런 다음 RdRp는 숙주 리보솜에 의한 번역을 위해 유전체를 전사하여 바이러스 단백질을 생성할 전령 RNA(mRNA)를 만들고, 자손 바이러스를 위해 유전체를 복제한다. 구대륙 한타바이러스는 골지체에서 조립되고 그곳에서 포막을 획득한 후, 세포막으로 운반되어 외포작용을 통해 세포를 빠져나간다. 신대륙 한타바이러스는 세포막 근처에서 조립되고 세포 표면에서 출아(budding)하여 세포를 빠져나갈 때 포막을 획득한다.
한타바이러스는 한국 전쟁 중에 처음 발견되었다. 전쟁 당시 HFRS는 한탄강 인근에 주둔한 군인들 사이에서 흔한 질병이었다. 최초의 한타바이러스는 1978년 대한민국에서 분리되었으며, 한탄 바이러스(Hantaan virus)로 명명되었다. 이 바이러스가 전쟁 중의 발병 원인임이 밝혀졌다. 몇 년 이내에 HFRS를 일으키는 다른 한타바이러스들이 유라시아 전역에서 발견되었다. 1982년에 세계보건기구(WHO)는 이 질환에 HFRS라는 이름을 부여했고, 1987년에 한타바이러스는 처음으로 독립된 속으로 분류되었다. 이들은 집합적으로 한탄 바이러스와 한탄강의 이름을 따서 명명되었다. 1993년 미국 포 코너스(Four Corners) 지역에서 HPS 발병이 발생하였고, 이는 병원성 신대륙 한타바이러스 및 한타바이러스에 의해 발생하는 두 번째 질병의 발견으로 이어졌다. 그 이후로 한타바이러스는 설치류뿐만 아니라 두더지, 땃쥐, 박쥐에서도 발견되었다.
질병
한타바이러스는 아프리카, 아시아, 유럽에서 주로 신증후출혈열(HFRS)을 일으키는 구대륙 한타바이러스(OWHV)와 아메리카 대륙에서 한타바이러스 폐증후군(HPS)과 연관된 신대륙 한타바이러스(NWHV)로 나뉜다. HFRS의 치명률은 1% 미만에서 15% 사이이며, HPS는 30~60%이다.[2][3][4][5] HFRS 증상의 중증도는 바이러스에 따라 다르다. 한탄 바이러스는 중증 HFRS, 서울 바이러스는 중등도 HFRS, 푸말라 바이러스는 경증 HFRS를 유발하며,[6] 도브라바-베오그라드 바이러스 감염은 유전자형에 따라 경증에서 중증까지 다양하다.[7] 푸말라 바이러스와 도브라바-베오그라드 바이러스에 의해 발생하는 경증 형태의 HFRS는 흔히 유행성 신병증(NE)으로 불린다.[8][9] 한타바이러스의 반복적인 감염은 관찰되지 않았으므로, 감염에서 회복되면 평생 면역을 얻을 가능성이 높다.[10][11]
HFRS는 발열기(febrile), 저혈압기(hypotensive), 핍뇨기(oliguria, 소변량 감소), 다뇨기(polyuria, 소변량 증가), 회복기(recovery)의 5단계가 특징이다. 증상은 보통 바이러스 노출 12~16일 후에 나타난다.[12] 급성 신장 질환은 신장 비대, 소변 내 단백질 과다(단백뇨), 소변 내 혈액(혈뇨)과 함께 발생한다. 다른 증상으로는 두통, 요통, 메스꺼움, 구토, 설사, 혈변, 피부의 반점 출현(점상출혈), 호흡기 출혈 등이 있다.[2][13] 신부전은 핍뇨로 이어지며, 신장 건강이 회복되면서 다뇨가 나타난다.[2][6] 회복에는 일반적으로 몇 달이 걸린다.[14] 경증의 경우 HFRS의 여러 단계를 구별하기 어렵거나 일부 단계가 없을 수 있으며,[15] 중증의 경우 단계들이 겹칠 수 있다.[6]
HPS는 주로 안데스 바이러스와 신 놈브레 바이러스의 두 가지 바이러스에 의해 발생한다. 이 질환은 전구기(초기), 심폐기, 회복기의 세 단계로 나뉜다. 증상은 바이러스 노출 후 약 1~8주 후에 나타난다. 초기 증상으로는 발열, 두통, 근육통, 숨가쁨(호흡 곤란), 낮은 혈소판 수(혈소판 감소증) 등이 있다. 심폐기 동안에는 심박수 증가(빈맥), 불규칙한 심장 박동(부정맥), 심인성 쇼크가 나타난다. 폐 모세혈관 누출은 급성 호흡곤란 증후군, 폐에 체액 축적(폐부종), 저혈압, 흉강에 체액 축적(흉수)으로 이어질 수 있다. 이러한 증상들은 돌연사를 유발할 수 있다.[2][5][16] 심폐기가 해결된 후 회복에는 일반적으로 3~6개월이 걸리며,[16] 이 기간 동안 다뇨증이 동반된다. HFRS는 신장 질환과 관련이 있고 HPS는 심폐 질환과 관련이 있지만, HFRS에 종종 HPS와 관련된 심폐 증상이 동반될 수 있으며, HPS에 종종 HFRS와 관련된 신장 증상이 동반될 수도 있다.[16][17]
전파



인간에게 질병을 일으키는 한타바이러스는 주로 설치류에 의해 전파된다. 설치류 내에서 한타바이러스는 대개 무증상의 지속적인 감염을 일으킨다. 감염된 동물은 대변, 소변, 타액,[6] 및 혈액[18]에서 나오는 에어로졸이나 비말, 오염된 음식 섭취, 피부나 털에서 떨어져 나온 바이러스 입자,[19] 털 고르기(grooming),[5] 또는 물림과 할큄 등을 통해 감염되지 않은 동물에게 바이러스를 퍼뜨릴 수 있다. 한타바이러스는 대변-구강 경로 및 임신 중 태반을 가로질러 어머니에서 아이로 전파될 수도 있다. 바이러스는 실온에서 10일,[2] 온대 환경에서 15일,[8] 섭씨 4도(화씨 39도)에서 18일 이상 생존할 수 있어 바이러스 전파에 도움이 된다.[2] 설치류의 번식과 확산에 유리한 환경 조건은 질병 전파를 증가시키는 것으로 알려져 있다.[3] 농촌 환경 거주, 비위생적인 환경, 숙주와 공유하는 환경과의 상호작용은 가장 큰 감염 위험 요인이며, 특히 등산객,[6] 농부, 임업 종사자,[8] 광업 종사자, 군인,[19][20] 동물학자에게 그 위험이 높다.[16]
2017년 북미의 한 유행에서, 서울 바이러스가 애완용 쥐와의 접촉을 통해 31명을 감염시켰다. 안데스 바이러스는 종종 연구자들에 의해 사람 간 전파가 가능한 유일한 한타바이러스로 알려져 있으며, 대개 감염된 사람과 밀접하게 접촉한 후 발생한다. 또한 사람의 타액, 기침과 재채기로 인한 공기 중 비말, 모유와 태반을 통해 신생아에게 전파되는 것으로 보고되었다.[2] 그러나 2021년의 한 체계적 문헌고찰에 따르면, 안데스 바이러스의 사람 간 전파는 증거로 강력하게 뒷받침되지는 않지만, 제한적인 상황,[3] 특히 성 파트너와 같은 밀접한 가족 접촉자 사이에서는 가능한 것으로 나타났다.[21] 푸말라 바이러스 역시 혈액 및 혈소판 수혈을 통해 사람 간에 전파될 수 있다는 의심이 있다.[22]
2026년 4월~5월, 오션와이드 엑스페디션(Oceanwide Expeditions)이 운영하는 네덜란드 선적 MV 혼디우스(MV Hondius)호에서 크루즈선에서 발생한 최초의 한타바이러스 발병이 기록되었다. 2026년 5월 2일, 승객과 승무원 147명을 태운 배에서 중증 호흡기 질환을 앓는 승객 집단이 WHO에 보고되었다. 2026년 5월 4일 기준으로 3명의 사망자를 포함해 7명의 환자가 확인되었다. 의사들은 관련된 바이러스 균주가 제한적인 사람 간 전파가 가능한 안데스 바이러스임을 확인했다. WHO는 전 세계 인구에 대한 위험을 낮음으로 평가했다.[23]
HFRS를 유발하는 한타바이러스는 진드기(mite)와 참진드기(tick)의 물림을 통해 전파될 수 있다.[24] 연구에 따르면 돼지는 심각한 증상 없이 한탄 바이러스에 감염될 수 있으며, 암퇘지는 태반을 통해 새끼에게 바이러스를 전파할 수 있다. 돼지에서 사람으로의 전파도 가능할 수 있는데, 한 양돈업자가 설치류나 진드기와의 접촉 없이 한타바이러스에 감염된 사례가 있다. 소, 사슴, 토끼에서 한탄 바이러스와 푸말라 바이러스가 검출되었고 고양이와 개에서 서울 바이러스에 대한 항체가 검출되었으나, 한타바이러스에 대한 이러한 숙주들의 역할은 알려져 있지 않다.[2] 다른 동물에서의 감염은 유전자 재조합(gene reassortment)을 통해 한타바이러스의 진화를 촉진할 잠재력이 있다.[16] 한타바이러스 중 일부는 설치류 외에도 두더지,[2][25] 땃쥐, 박쥐 등 식충성 소형 포유류에서 발견된다.[9][16] 감염의 지표인 한타바이러스 항원은 다양한 조류 종에서도 검출되었다.[24]
인간이 구축한 환경은 한타바이러스 전파에 중요하다. 삼림 벌채와 과도한 농업은 설치류의 자연 서식지를 파괴할 수 있다.[16] 농경지의 확장은 포식자 개체 수 감소와 관련이 있으며, 이는 한타바이러스 숙주 종이 농장 단일 재배지를 둥지 및 먹이 찾기 장소로 이용할 수 있게 한다. 설치류의 자연 서식지와 가까운 곳에 지어진 농업 현장은 동물 사료에 이끌릴 수 있어 설치류의 증식을 촉진할 수 있다.[18][26] 특히 고체 폐기물 관리가 부실한 지역의 하수도 및 빗물 배수 시스템에는 설치류가 서식할 수 있다. 해상 무역과 여행도 한타바이러스 확산에 영향을 미쳤다.[18] 도시 거주가 한타바이러스 발생률을 증가시키는지 감소시키는지에 대한 연구 결과는 일관되지 않다.[26] 과거 한타바이러스 감염을 보여주는 혈청유병률(seroprevalence)은 설치류 노출이 많은 직업 및 지역에서 일관되게 높게 나타난다.[21] 전쟁터, 군부대, 난민 캠프의 열악한 생활 조건은 군인과 난민을 감염 위험에 노출시킨다.[20]
환경

한타바이러스를 매개하는 설치류 종은 사막과 유사한 생물 군계, 적도 및 열대 우림, 늪, 사바나, 들판, 염습지 등 다양한 서식지에 거주한다.[18] 숙주 종 내 한타바이러스 혈청유병률은 검사 방법 및 위치에 따라 아메리카 대륙에서 5.9%~38%, 전 세계적으로 3%~약 19%의 범위로 관찰되었다.[19][27] 대한민국과 같은 일부 지역에서는 한타바이러스 순환을 감시하기 위해 야생 설치류를 정기적으로 포획한다.[4] 따뜻한 기후에서 높은 습도는 식물 성장에 긍정적인 영향을 미쳐 먹이 가용성을 높임으로써 설치류 개체군에 유익할 수 있다.[18] 삼림 면적의 증가는 특히 유럽에서 한타바이러스 발생률 증가와 관련이 있다.[26]
기후 변화와 환경 파괴는 설치류 숙주와 인간 사이의 접촉 부위를 늘려 한타바이러스 노출 가능성을 증가시킨다. 1992~1993년의 엘니뇨 온난화 기간으로 인한 폭우 직후에 발생한 미국 1993년 포 코너스 발병이 그 예이다. 이로 인해 설치류의 먹이 공급이 크게 증가하여 개체 수가 급증했고, 당시 발병을 일으킨 한타바이러스의 확산을 촉진했다.[18][19][28]
강수량은 다양한 패턴으로 한타바이러스 발생률과 일관된 연관성을 갖는다. 폭우는 그 이후 수개월 동안 발병의 위험 요인이지만,[10] 설치류 굴과 둥지를 침수시켜 발생률에 부정적인 영향을 미칠 수도 있다.[28] 우기와 건기가 있는 지역에서는 건기보다 우기에 감염이 더 흔하다.[18] 낮은 강수량과 가뭄은 설치류 개체 수를 감소시키므로 발생률 감소와 연관이 있지만,[28] 가뭄이나 홍수로 인한 설치류 개체군의 이동은 설치류-인간 상호작용 및 감염 증가로 이어질 수 있다.[18] 그러나 유럽에서는 강수량과 질병 발생률 사이에 연관성이 발견되지 않았다.[28]
온도는 한타바이러스 전파에 다양한 영향을 미친다. 높은 온도는 바이러스 생존에 불리한 환경을 조성하고 신열대구(Neotropic) 설치류의 활동 수준을 감소시키지만, 설치류가 더위를 피해 인간의 거주 환경으로 피신하도록 만들 수 있으며 에어로졸 생성에 유리하다.[16][18] 낮은 온도는 숙주 외부에서 바이러스의 생존 기간을 연장할 수 있다.[18] 높은 겨울 평균 기온은 푸말라 바이러스의 자연 숙주인 유럽애기들쥐의 생존 감소와 관련이 있지만, 중국에서는 한탄 바이러스의 자연 숙주인 등줄쥐의 생존 증가와 관련이 있다.[28] 덥든 춥든 극한의 온도는 질병 발생률을 낮추는 것과 관련이 있다.[10]
유전체 및 구조
한타바이러스의 유전체는 대(L), 중(M), 소(S) 분절의 세 부분으로 나뉜다. 각 부분은 단일 가닥 음성 방향 RNA 가닥으로 총 10,000~15,000개의 뉴클레오타이드로 구성된다.[5] 이 분절들은 유전체 말단의 비공유 결합을 통해 원형을 형성한다.[29] L 분절은 길이가 약 6.6 킬로베이스(kb)이며,[19] 바이러스 RNA의 전사 및 복제를 매개하는 바이러스 RNA 의존성 RNA 중합효소(RdRp)를 암호화한다. M 분절은 길이가 약 3.7 kb이며,[19] 함께 번역되고 분할되어 Gn 및 Gc가 되는 당단백질 전구체를 암호화한다. Gn과 Gc는 세포 수용체에 결합하고 면역 반응을 조절하며 방어 항체를 유도한다. S 분절은 길이가 약 2.1 kb이며,[19] 바이러스 RNA에 결합하여 이를 보호하는 뉴클레오캡시드 단백질 N을 암호화한다. 일부 오르토한타바이러스 S 분절의 N 유전자 내에 있는 열린 해독틀(open reading frame)[30]은 숙주 세포에서 인터페론 생성을 억제하는 비구조 단백질 NS를 암호화하기도 한다. 유전체 양 끝의 번역되지 않은 영역은 고도로 보존되어 있으며 유전체의 복제 및 전사에 참여한다.[2][5][6]
개별 한타바이러스 입자(비리온)는 대개 구형이지만 타원형, 다형성,[31] 또는 관형일 수도 있다.[5] 비리온의 직경은 70~350 나노미터이다.[19] 비리온의 바깥쪽 부분은 약 5nm 두께의 지질 포막이다. 포막에는 표면 스파이크 당단백질인 Gn과 Gc가 내장되어 있으며,[2] 이들은 격자 모양으로 배열되어 있다.[19] 각 표면 스파이크는 4회전 대칭 구조를 갖는 Gn과 Gc의 사량체(각각 4개 단위)로 구성되며 포막에서 약 10nm 바깥으로 뻗어 나온다.[19] Gn은 스파이크의 자루를 형성하고 Gc는 머리 부분을 형성한다.[5] 포막 내부에는 여러 카피의 뉴클레오캡시드 단백질 N으로 구성된 나선형 뉴클레오캡시드가 있으며, 이는 바이러스 유전체에 부착되어 리보핵단백질(RNP) 복합체를 형성한다. 각 RNP 복합체에는 RdRp 사본이 부착되어 있다.[2] 한타바이러스는 비리온을 구조화하는 데 도움을 주는 기질 단백질을 암호화하지 않으므로, 표면 단백질이 어떻게 대칭적인 격자 구조의 구형으로 조직되는지는 아직 밝혀지지 않았다.[32]
생활사

혈관 내피세포와 대식세포는 한타바이러스에 일차적으로 감염되는 세포이다.[9] 족세포, 관상 세포, 수지상 세포, 림프구도 감염될 수 있다.[2][16] 숙주 세포로의 부착 및 진입은 바이러스 당단백질 스파이크가 숙주 세포 수용체, 특히 베타-3 인테그린에 결합함으로써 매개된다. 붕괴 촉진 인자, 보체 수용체, 그리고 신대륙 한타바이러스의 경우 프로토카데린-1이 부착에 관여하는 것으로 제안되었다.[16][32] 부착 후, 한타바이러스는 대음세포작용, 클라트린 비의존성 수용체 매개 내포작용, 콜레스테롤 또는 카베올라 의존성 내포작용 등 여러 가지 방법으로 세포에 진입한다.[2][5][16] 구대륙 한타바이러스는 클라트린 의존성 내포작용을 사용하는 반면, 신대륙 한타바이러스는 클라트린 비의존성 내포작용을 사용한다.[16][22][33]
세포 내로 진입한 후 비리온은 초기 엔도솜, 그 후 후기 엔도솜 및 리소좀 구획으로 운반되는 소포를 형성한다. 그런 다음 pH가 떨어지면서 바이러스 포막이 엔도솜 또는 리소좀과 융합된다.[19][22][33] 이 융합을 통해 바이러스 리보핵단백질 복합체가 세포질로 방출되어 RdRp에 의한 전사 및 복제가 시작된다.[2][16][19] RdRp는 바이러스 -ssRNA를 상보적인 양성 가닥으로 전사한 다음, 바이러스 단백질을 생성하기 위해 숙주 리보솜이 번역할 mRNA를 준비할 수 있도록 숙주 전령 RNA(mRNA)의 5′("5 프라임") 끝을 가로챈다.[5][19] 상보적 RNA 가닥은 N 단백질에 둘러싸여 RNP를 형성하는 유전체 사본을 생산하는 데에도 사용된다.[2][16][19]
비리온 조립 과정에서 당단백질 전구체는 소포체 내에서 숙주 세포의 신호 펩티데이스에 의해 분할되어 Gn 및 Gc 당단백질이 된다.[2][5] Gn과 Gc는 N-글리칸 사슬에 의해 변형되는데, 이는 스파이크 구조를 안정화하고 구대륙 한타바이러스의 경우 골지체에서,[2] 신대륙 한타바이러스의 경우 세포막에서의[16] 조립을 돕는다. 구대륙 한타바이러스는 골지체에서 바이러스 포막을 획득하고 소포에 담겨 세포막으로 운반된 후 외포작용을 통해 세포를 빠져나간다. 반면에 신대륙 한타바이러스 RNP는 세포막으로 수송되며, 그곳에서 세포 표면으로부터 출아하여 포막을 획득하고 세포를 떠난다.[16][19][22]
진화
한타바이러스가 진화하는 가장 일반적인 형태는 단일 뉴클레오타이드 치환, 삽입 및 결실을 통한 돌연변이이다.[2] 한타바이러스는 대개 각각의 자연 숙주 종에 국한되어 숙주와 함께 진화하지만,[2] 이러한 일-종-일-한타바이러스(one-species-one-hantavirus) 관계가 모든 한타바이러스에 해당하는 것은 아니다. 한타바이러스의 정확한 진화 역사는 유전체 재편성, 숙주 전파 및 숙주 전환의 많은 사례로 인해 파악이 어렵다.[34] 종 내에서는 지리가 한타바이러스의 진화에 영향을 미쳤다. 예를 들어, 한탄 바이러스와 서울 바이러스는 모두 그들의 지리적 분포에 상응하는 여러 계통을 형성했다.[2]
한타바이러스는 분절형 유전체를 가지고 있기 때문에 서로 다른 바이러스의 분절이 결합하여 새로운 바이러스를 형성할 수 있는 유전자 재조합 및 유전자 재편성이 가능하다. 이는 자연에서 자주 발생하며 한타바이러스가 여러 숙주와 생태계에 적응하는 것을 촉진한다. 구대륙 한타바이러스(OWHV) S 및 M 분절의 재조합은 일반적으로 동일 종 내 바이러스 간에 관찰되지만 종 간에도 발생할 수 있다. 신대륙 한타바이러스(NWHV) S 및 M 분절의 재편성은 설치류에서 관찰되었다. 2005-2009년 설치류에서 분리된 푸말라 바이러스 중 19.1%가 재편성된 것으로 확인되었다.[2][35] 두 부모 바이러스로부터 동일한 분절 두 개를 가지게 되는 이배체 자손 비리온도 가능하다.[25]
분류
오르토한타바이러스(Orthohantavirus)는 모든 한타바이러스를 포함하는 한타바이러스과(Hantaviridae) 계통에 속한다. 이 속에는 37개의 종이 있으며, 종을 대표하는 바이러스(exemplar virus)와 함께 아래에 나열되어 있다. 일반적으로 종 이름은 대표 바이러스 이름에 접미사 -ense를 붙여 명명된다.[29][36]
- Orthohantavirus andesense, 안데스 바이러스(Andes virus)
- Orthohantavirus artybashense, 아르티바쉬 바이러스(Artybash virus)
- Orthohantavirus asamaense, 아사마 바이러스(Asama virus)
- Orthohantavirus asikkalaense, 아시칼라 바이러스(Asikkala virus)
- Orthohantavirus bayoui, 바유 바이러스(Bayou virus)
- Orthohantavirus boweense, 보웨 바이러스(Bowé virus)
- Orthohantavirus brugesense, 브루게스 바이러스(Bruges virus)
- Orthohantavirus caobangense, 까오방 바이러스(Cao Bằng virus)
- Orthohantavirus carrizalense, 카리살 바이러스(Carrizal virus)
- Orthohantavirus chocloense, 초클로 바이러스(Choclo virus)
- Orthohantavirus dabieshanense, 다비에샨 바이러스(Dàbiéshān virus)
- Orthohantavirus delgaditoense, 카뇨 델가디토 바이러스(Caño Delgadito virus)
- Orthohantavirus dobravaense, 도브라바-베오그라드 바이러스(Dobrava-Belgrade virus)[note 1]
- Orthohantavirus fugongense, 푸궁 바이러스(Fúgòng virus)
- Orthohantavirus hantanense, 한탄 바이러스(Hantaan virus)
- Orthohantavirus jejuense, 제주 바이러스(Jeju virus)
- Orthohantavirus kenkemeense, 켄케메 바이러스(Kenkeme virus)
- Orthohantavirus khabarovskense, 하바롭스크 바이러스(Khabarovsk virus)
- Orthohantavirus lankaense, 랑카 바이러스(Lanka virus)
- Orthohantavirus luxiense, 루시 바이러스(Lúxī virus)
- Orthohantavirus mamorense, 리오 마모레 바이러스(Rio Mamoré virus)
- Orthohantavirus maporalense, 마포랄 바이러스(Maporal virus)
- Orthohantavirus montanoense, 몬타뇨 바이러스(Montaño virus)
- Orthohantavirus nigrorivense, 블랙 크리크 운하 바이러스(Black Creek Canal virus)
- Orthohantavirus ozarkense, 오자크 바이러스(Ozark virus)
- Orthohantavirus prospectense, 프로스펙트 힐 바이러스(Prospect Hill virus)
- Orthohantavirus puumalaense, 푸말라 바이러스(Puumala virus)
- Orthohantavirus rockportense, 록포트 바이러스(Rockport virus)
- Orthohantavirus sagercreekense 세이거 크릭 바이러스(Sager Creek virus)
- Orthohantavirus sangassouense, 상가수 바이러스(Sangassou virus)
- Orthohantavirus seoulense, 서울 바이러스(Seoul virus)
- Orthohantavirus sinnombreense, 신 놈브레 바이러스(Sin Nombre virus)
- Orthohantavirus tatenalense, 타테날레 바이러스(Tatenale virus)
- Orthohantavirus thailandense, 안조조로베 바이러스(Anjozorobe virus)와 태국 바이러스(Thailand virus)를 포함함[note 2]
- Orthohantavirus tigrayense, 티그레이 바이러스(Tigray virus)
- Orthohantavirus tulaense, 툴라 바이러스(Tula virus)
- Orthohantavirus wufangense, 우펑 소코고슴도치 오르토한타바이러스 1(Wùfeng Chodsigoa smithii orthohantavirus 1)
많은 다른 한타바이러스들이 분류되지 않은 채 남아있으나, 이들 중 일부는 다른 바이러스들의 분리주일 수 있다.[29][37]
- Academ virus
- Adler virus
- Alto Paraguay virus
- Amga virus / Seewis virus[38]
- Anajatuba virus
- Ash River virus
- Asturias virus
- Azagny virus
- Belgrade virus
- Biya river virus
- Bloodland Lake virus
- Blue River virus
- Boginia virus
- Calabazo virus
- Camp Ripley virus
- Castelo dos Sonhos virus
- CGRn9415 virus
- Dode virus
- El Moro Canyon virus
- Fox Creek virus
- Fusong virus
- Gou virus (Gōu virus)
- hantavirus sp. strain Tamarin/BRA/SM22/2014
- HoJo virus
- Iamonia virus
- Isla Vista virus
- Jemez Springs virus
- Jerboa hantavirus
- Jurong virus
- Kielder hantavirus
- Laguna Negra virus
- Landiras virus
- Leakey virus
- Lechiguanas virus
- Liánghé virus
- Lohja virus
- Malacky virus
- Muleshoe virus
- Necocli virus
- Orán virus
- Oxbow virus
- Playa de Oro virus
- Powell Butte virus
- Prairie vole virus
- Qiān Hú Shān virus / Qiāndǎo Lake virus
- Rio Mearim virus
- Río Segundo virus
- Sapporo rat virus
- Sarufutsu virus
- Serang virus
- Shěnyáng virus
- Taimyr virus
- Tanganya virus
- Tualatin River virus
- Uurainen virus
- Vladivostok virus
- Yakeshi virus
- Yuánjiāng virus
역사
한타바이러스성 출혈 질환은 아마도 기원전 475~221년 전국시대 고대 중국의 의학 서적인 황제내경(Huangdi Neijing)에서 처음 묘사되었을 것이다.[34] 한타바이러스는 미국 남북 전쟁 중 군인들과 제1차 세계 대전 당시 벨기에 플랑드르의 영국 군인들 사이에서 발생한 "참호 신염(trench nephritis)"의 원인으로 제시되었다.[34] 이 질병은 풍토병이었을 가능성이 높은 동아시아에서도 언급되었으며, 1913~1914년 블라디보스토크에서 과학적으로 처음 기술되었다. 1942년 제2차 세계 대전 중에 한타바이러스 감염의 특징적인 증상을 동반한 질병이 핀란드 동부 라플란드의 살라(Salla)에 주둔한 독일군 및 핀란드 군인들 사이에서 발생했다. 이 발병은 1980년에 유럽애기들쥐에 의해 전파되는 바이러스가 원인인 것으로 보고되었으며, 푸말라 바이러스(Puumala virus)로 명명되었다.[20] 또한 전쟁 중 만주에 주둔했던 약 10,000명의 일본군 병사들이 HFRS에 걸렸다.[6]
한국 전쟁 중 한탄강 인근에 주둔한 유엔군 사이에서 약 3,200건[20]의 HFRS 사례가 발생했으며,[32] 이 질병은 1951년 처음 확인되어[2] "한국형 출혈열(Korean hemorrhagic fever)" 및 "유행성 출혈열(epidemic hemorrhagic fever)"이라는 이름이 붙여졌다.[34] 전쟁 후 1976년 한국에서 이호왕(Ho Wang Lee)[14] 박사는 등줄쥐를 검사하여 그 쥐의 폐에서 나온 항원이 전쟁 생존자의 혈청에 있는 항체와 반응함을 보여주었다.[34] 1978년에 바이러스가 최초로 분리되었고 강의 이름을 따서 한탄 바이러스(Hantaan virus)로 명명되었다.[13] 후향적 분석을 통해 한탄 바이러스가 전쟁 당시 유행을 일으킨 원인으로 밝혀졌다.[20] 그 후 유라시아 전역에서 HFRS를 유발하는 다른 한타바이러스가 발견되었다. 이 질병은 다양한 이름으로 불렸으므로 1982년에 세계보건기구(WHO)는 공식적으로 "신증후출혈열(hemorrhagic fever with renal syndrome)"이라는 이름을 부여했다.[6][34] 1985년에 이 바이러스 그룹은 한탄 바이러스의 이름을 따서 "한타바이러스"로 명명되었고,[31] 1987년에 당시 부니아바이러스과(Bunyaviridae) 내에 이들을 수용하기 위한 한타바이러스속(Hantavirus)이 확립되었다.[39]
최초의 한타바이러스 백신인 한타박스(Hantavax)는 1990년 이호왕 박사가 이끄는 연구팀에 의해 개발되었다.[40] 이 백신은 한탄 바이러스(HTNV) 및 서울 바이러스(SEOV)와 같이 동북아시아 지역의 한타바이러스 계통에만 효과가 있다. 유럽이나 미국에서는 사용이 승인되지 않았다.[41]
1993년 미국 포 코너스(Four Corners) 지역에서 치명률이 매우 높은 급성 호흡곤란 증후군이 발병했다. 이 발병은 현재 신 놈브레 바이러스(Sin Nombre virus)로 명명된 한타바이러스에 의해 발생한 것으로 밝혀졌으며, 아메리카 대륙에서 병원성 한타바이러스가 처음으로 확인된 사례이자 한타바이러스가 일으키는 새로운 질병의 발견을 의미했다. 새로운 질병은 한타바이러스 폐증후군(Hantavirus Pulmonary Syndrome)으로 명명되었다. 이후 몇 년 동안 아메리카 대륙에서 수많은 다른 한타바이러스가 발견되었으며,[5][34] 이 중에는 사람 간 전파가 가능하다고 주장되는 안데스 바이러스도 포함되어 있다.[3] 그러나 HFRS는 HPS보다 훨씬 더 흔하게 발생하는데, HFRS 환자는 매년 100,000명 이상 발생하는 반면[26] HPS 사례는 매년 수백 건에 불과하다.[42]
시간이 지나면서 수백 개의 부니아바이러스(bunyavirus)가 발견되었으나 부니아바이러스과(Bunyaviridae) 내의 속들에는 이들을 모두 수용할 수 없었다. 이를 해결하기 위해 2017년에 부니아바이러스는 목(order) 단계인 부니아바이러스목(Bunyavirales)으로 격상되었고, 한타바이러스는 다른 부니아바이러스 속들과 함께 과(family) 단계로 승격되었다. 한타바이러스(한타비리드, hantavirids)는 이제 한타바이러스과(Hantaviridae) 계통의 구성원을 지칭하게 되었다. 기존의 한타바이러스속(Hantavirus)은 과(family)의 구성원들과 구별하기 위해 오르토한타바이러스속(Orthohantavirus)으로 개명되었으며, 이 속의 구성원들은 종종 오르토한타바이러스로 불린다. 2019년에 설치류 이외의 한타바이러스를 분류하기 위해 추가적인 속과 아과가 만들어졌고,[34] 2023년에는 한타바이러스에 대해 이명법(binomial nomenclature)이 채택되었다.[2]
주해
각주
- ↑ “Hantavirus” (영어). 《www.who.int》. 2026년 5월 6일에 확인함.
- ↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 너 더 러 머 버 서 어 저 처 Chen R, Gong H, Wang X, Sun M, Ji Y, Tan S, Chen J, Shao J, Liao M (2023년 8월 8일). “Zoonotic Hantaviridae with Global Public Health Significance”. 《Viruses》 15 (8): 1705. doi:10.3390/v15081705. PMC 10459939
|pmc=값 확인 필요 (도움말). PMID 37632047. - ↑ 가 나 다 라 Toledo J, Haby MM, Reveiz L, Sosa Leon L, Angerami R, Aldighieri S (2022년 10월 17일). “Evidence for Human-to-Human Transmission of Hantavirus: A Systematic Review”. 《J Infect Dis》 226 (8): 1362–1371. doi:10.1093/infdis/jiab461. PMC 9574657. PMID 34515290.
- ↑ 가 나 Kim WK, Cho S, Lee SH, No JS, Lee GY, Park K, Lee D, Jeong ST, Song JW (2021년 1월 8일). “Genomic Epidemiology and Active Surveillance to Investigate Outbreaks of Hantaviruses”. 《Front Cell Infect Microbiol》 10. doi:10.3389/fcimb.2020.532388. PMC 7819890. PMID 33489927.
- ↑ 가 나 다 라 마 바 사 아 자 차 카 Jacob AT, Ziegler BM, Farha SM, Vivian LR, Zilinski CA, Armstrong AR, Burdette AJ, Beachboard DC, Stobart CC (2023년 11월 9일). “Sin Nombre Virus and the Emergence of Other Hantaviruses: A Review of the Biology, Ecology, and Disease of a Zoonotic Pathogen”. 《Biology》 12 (11): 1143. doi:10.3390/biology12111413. PMC 10669331
|pmc=값 확인 필요 (도움말). PMID 37998012. - ↑ 가 나 다 라 마 바 사 아 Tariq M, Kim DM (March 2022). “Hemorrhagic Fever with Renal Syndrome: Literature Review, Epidemiology, Clinical Picture and Pathogenesis”. 《Infect Chemother》 54 (1): 1–19. doi:10.3947/ic.2021.0148. PMC 8987181. PMID 35384417.
- ↑ Klempa B, Avsic-Zupanc T, Clement J, Dzagurova TK, Henttonen H, Heyman P, Jakab F, Kruger DH, Maes P, Papa A, Tkachenko EA, Ulrich RG, Vapalahti O, Vaheri A (2013). “Complex evolution and epidemiology of Dobrava-Belgrade hantavirus: definition of genotypes and their characteristics”. 《Arch Virol》 158 (3): 521–529. doi:10.1007/s00705-012-1514-5. PMC 3586401. PMID 23090188.
- ↑ 가 나 다 Riccò M, Peruzzi S, Ranzieri S, Magnavita N (2021년 10월 25일). “Occupational Hantavirus Infections in Agricultural and Forestry Workers: A Systematic Review and Metanalysis”. 《Viruses》 13 (11): 2150. doi:10.3390/v13112150. PMC 8621010. PMID 34834957.
- ↑ 가 나 다 Afzal S, Ali L, Batool A, Afzal M, Kanwal N, Hassan M, Safdar M, Ahmad A, Yang J (2023년 10월 12일). “Hantavirus: an overview and advancements in therapeutic approaches for infection”. 《Front Microbiol》 14. doi:10.3389/fmicb.2023.1233433. PMC 10601933
|pmc=값 확인 필요 (도움말). PMID 37901807. - ↑ 가 나 다 Hansen A, Cameron S, Liu Q, Sun Y, Weinstein P, Williams C, Han GS, Bi P (April 2015). “Transmission of haemorrhagic fever with renal syndrome in china and the role of climate factors: a review”. 《Int J Infect Dis》 33: 212–218. doi:10.1016/j.ijid.2015.02.010. hdl:2440/94644. PMID 25704595.
- ↑ Krüger DH, Schönrich G, Klempa B (June 2011). “Human pathogenic hantaviruses and prevention of infection”. 《Hum Vaccin》 7 (6): 685–693. doi:10.4161/hv.7.6.15197. PMC 3219076. PMID 21508676.
- ↑ Zhang Y, Ma R, Wang Y, Sun W, Yang Z, Han M, Han T, Wu XA, Liu R (2021년 9월 30일). “Viruses Run: The Evasion Mechanisms of the Antiviral Innate Immunity by Hantavirus”. 《Front Microbiol》 12. doi:10.3389/fmicb.2021.759198. PMC 8516094. PMID 34659193.
- ↑ 가 나 Sehgal A, Mehta S, Sahay K, Martynova E, Rizvanov A, Baranwal M, Chandy S, Khaiboullina S, Kabwe E, Davidyuk Y (2023년 2월 18일). “Hemorrhagic Fever with Renal Syndrome in Asia: History, Pathogenesis, Diagnosis, Treatment, and Prevention”. 《Viruses》 15 (2): 561. doi:10.3390/v15020561. PMC 9966805. PMID 36851775.
- ↑ 가 나 Lupuşoru G, Lupuşoru M, Ailincăi I, Bernea L, Berechet A, Spătaru R, Ismail G (September 2021). “Hanta hemorrhagic fever with renal syndrome: A pathology in whose diagnosis kidney biopsy plays a major role (Review)”. 《Exp Ther Med》 22 (33). doi:10.3892/etm.2021.10416. PMC 8311249. PMID 34345266.
- ↑ Avšič-Županc T, Saksida A, Korva M (April 2019). “Hantavirus infections”. 《Clin Microbiol Infect》 21S: e6–e16. doi:10.1111/1469-0691.12291. PMID 24750436.
- ↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 너 Koehler FC, Di Cristanziano V, Späth MR, Hoyer-Allo KJ, Wanken M, Müller RU, Burst V (2022년 1월 29일). “The kidney in hantavirus infection-epidemiology, virology, pathophysiology, clinical presentation, diagnosis and management”. 《Clin Kidney J》 15 (7): 1231–1252. doi:10.1093/ckj/sfac008. PMC 9217627. PMID 35756741.
- ↑ Noack D, Goeijenbier M, Reusken CB, Koopmans MP, Rockx BH (2020년 8월 4일). “Orthohantavirus Pathogenesis and Cell Tropism”. 《Front Cell Infect Microbiol》 10. doi:10.3389/fcimb.2020.00399. PMC 7438779. PMID 32903721.
- ↑ 가 나 다 라 마 바 사 아 자 차 Douglas KO, Payne K, Sabino-Santos G J, Agard J (2021년 12월 23일). “Influence of Climatic Factors on Human Hantavirus Infections in Latin America and the Caribbean: A Systematic Review”. 《Pathogens》 11 (1): 15. doi:10.3390/pathogens11010015. PMC 8778283. PMID 35055965. 밴쿠버 양식 오류 (도움말)
- ↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 D'Souza MH, Patel TR (2020년 8월 7일). “Biodefense Implications of New-World Hantaviruses”. 《Front Bioeng Biotechnol》 8. doi:10.3389/fbioe.2020.00925. PMC 7426369. PMID 32850756.
- ↑ 가 나 다 라 마 Mustonen J, Henttonen H, Vaheri A (2024년 2월 27일). “Hantavirus Infections among Military Forces”. 《Mil Med》 189 (3–4): 551–555. doi:10.1093/milmed/usad261. PMC 10898924
|pmc=값 확인 필요 (도움말). PMID 37428512. - ↑ 가 나 Tortosa F, Perre F, Tognetti C, Lossetti L, Carrasco G, Guaresti G, Iglesias A, Espasandin Y, Izcovich A (2024년 9월 19일). “Seroprevalence of hantavirus infection in non-epidemic settings over four decades: a systematic review and meta-analysis”. 《BMC Public Health》 24 (1). doi:10.1186/s12889-024-20014-w. PMC 11414058
|pmc=값 확인 필요 (도움말). PMID 39300359. - ↑ 가 나 다 라 Meier K, Thorkelsson SR, Quemin ER, Rosenthal M (2021년 8월 6일). “Hantavirus Replication Cycle-An Updated Structural Virology Perspective”. 《Viruses》 13 (8): 1561. doi:10.3390/v13081561. PMC 8402763. PMID 34452426.
- ↑ [[1](https://www.who.int/emergencies/disease-outbreak-news/item/2026-DON599) “Hantavirus cluster linked to cruise ship travel, Multi-country”]
|url=값 확인 필요 (도움말). 《World Health Organization》. 2026년 5월 4일. 2026년 5월 6일에 확인함. - ↑ 가 나 Tkachenko E, Balkina A, Trankvilevsky D, Kolyasnikova N, Teodorovich R, Vorovich M, Popova Y, Kurashova S, Egorova M, Belyakova A, Tkachenko P, Ishmukhametov A, Dzagurova T (2024년 8월 13일). “The Specificity of Epizootic and Epidemiological Processes in Natural Foci of Hemorrhagic Fever with Renal Syndrome and Tick-Borne Encephalitis in Russia, as the Basis for the Prospects of Creating a Combined Vaccine for the Prevention of These Infections”. 《Viruses》 16 (8): 1292. doi:10.3390/v16081292. PMC 11359185
|pmc=값 확인 필요 (도움말). PMID 39205266. - ↑ 가 나 Klempa B (October 2018). “Reassortment events in the evolution of hantaviruses”. 《Virus Genes》 54 (5): 638–646. doi:10.1007/s11262-018-1590-z. PMC 6153690. PMID 30047031.
- ↑ 가 나 다 라 Moirano G, Botta A, Yang M, Mangeruga M, Murray K, Vineis P (July 2024). “Land-cover, land-use and human hantavirus infection risk: a systematic review”. 《Pathog Glob Health》 118 (5): 361–375. doi:10.1080/20477724.2023.2272097. PMC 11338209
|pmc=값 확인 필요 (도움말). PMID 37876214. - ↑ Obando-Rico CJ, Valencia-Grajales YF, Bonilla-Aldana DK (January–February 2023). “Prevalence of orthohantavirus in rodents: A systematic review and meta-analysis”. 《Travel Med Infect Dis》 51. doi:10.1016/j.tmaid.2022.102504. PMID 36402291.
- ↑ 가 나 다 라 마 Tian H, Stenseth NC (2021년 2월 21일). “The ecological dynamics of hantavirus diseases: From environmental variability to disease prevention largely based on data from China”. 《PLOS Negl Trop Dis》 13 (2). doi:10.1371/journal.pntd.0006901. PMC 6383869. PMID 30789905.
- ↑ 가 나 다 [[2](https://ictv.global/report/chapter/hantaviridae/hantaviridae/mammantavirinae/orthohantavirus) “Genus: Orthohantavirus”]
|url=값 확인 필요 (도움말). 《ictv.global》. International Committee on Taxonomy of Viruses. 2025년 1월 10일에 확인함. - ↑ Bae JY, Kim JI, Park MS, Lee GE, Park H, Song KJ, Park MS (2021년 5월 18일). “The Immune Correlates of Orthohantavirus Vaccine”. 《Vaccines》 9 (5): 518. doi:10.3390/vaccines9050518. PMC 8157935. PMID 34069997.
- ↑ 가 나 Deng X, Tian S, Yu Z, Wang L, Liang R, Li Y, Xiang R, Jiang S, Ying T, Yu F (July–August 2020). “Development of small-molecule inhibitors against hantaviruses”. 《Microbes Infect》 22 (6–7): 272–277. doi:10.1016/j.micinf.2020.05.011. PMID 32445882.
- ↑ 가 나 다 Guardado-Calvo P, Rey FA (October 2021). “The surface glycoproteins of hantaviruses”. 《Curr Opin Virol》 50: 87–94. doi:10.1016/j.coviro.2021.07.009. PMID 34418649.
- ↑ 가 나 LaPointe A, Gale M J, Kell AM (2023년 5월 9일). “Orthohantavirus Replication in the Context of Innate Immunity”. 《Viruses》 15 (5): 1130. doi:10.3390/v15051130. PMC 10220641
|pmc=값 확인 필요 (도움말). PMID 37243216. 밴쿠버 양식 오류 (도움말) - ↑ 가 나 다 라 마 바 사 아 Kuhn JH, Schmaljohn CS (2023년 2월 28일). “A Brief History of Bunyaviral Family Hantaviridae”. 《Diseases》 11 (1): 38. doi:10.3390/diseases11010038. PMC 10047430
|pmc=값 확인 필요 (도움말). PMID 36975587. - ↑ Kabwe E, Davidyuk Y, Shamsutdinov A, Garanina E, Martynova E, Kitaeva K, Malisheni M, Isaeva G, Savitskaya T, Urbanowicz RA, Morzunov S, Katongo C, Rizvanov A, Khaiboullina S (2020년 9월 22일). “Orthohantaviruses, Emerging Zoonotic Pathogens”. 《Pathogens》 9 (9): 775. doi:10.3390/pathogens9090775. PMC 7558059. PMID 32971887.
- ↑ “Virus Taxonomy: 2024 Release”. International Committee on Taxonomy of Viruses. 2025년 3월 17일에 확인함.
- ↑ Kuhn JH, Bradfute SB, Calisher CH, Klempa B, Klingström J, Laenen L, Palacios G, Schmaljohn CS, Tischler N, Maes P (2023년 6월 23일). [[3](https://ictv.global/ictv/proposals/2023.035M.Hantaviridae_reorg.zip) “Reevaluate and reorganize family Hantaviridae (order Bunyavirales)”]
|url=값 확인 필요 (도움말) (docx). 《ictv.global》. International Committee on Taxonomy of Viruses. 2025년 1월 10일에 확인함. - ↑ [[4](https://ictv.global/taxonomy/taxondetails?taxnode_id=202200021&taxon_name=Orthohantavirus%20seewisense) “History of the taxon: Species: Orthohantavirus seewisense (2022 Release, MSL #38)”]
|url=값 확인 필요 (도움말). 《ictv.global》. International Committee on Taxonomy of Viruses. 2025년 1월 10일에 확인함. - ↑ 인용 오류: 잘못된
<ref>태그;orthohistory이라는 이름을 가진 ref에 텍스트가 없습니다 - ↑ “Previous Laureates - HOAM”. 《www.hoamfoundation.org》. 2026년 5월 6일에 확인함.
- ↑ Schmaljohn, C. S. (2012). “Vaccines for hantaviruses: Progress and issues”. 《Expert Review of Vaccines》 11 (5): 511–513. doi:10.1586/ERV.12.15. PMID 22827236. S2CID 27574264. 2017년 7월 3일에 원본 문서 (PDF)에서 보존된 문서.
- ↑ Engdahl TB, Crowe Jr JE (2020년 7월 15일). “Humoral Immunity to Hantavirus Infection”. 《mSphere》 15 (4). doi:10.1128/mSphere.00482-20. PMC 7364217. PMID 32669473.
외부 링크
- [[5](https://www.cdc.gov/hantavirus/pdf/hps_brochure.pdf) 미국 질병통제예방센터(CDC)의 한타바이러스 팩트 시트 (PDF)]
- [[6](https://www.cdc.gov/ncidod/diseases/hanta/hps/noframes/phys/technicalinfoindex.htm) 미국 질병통제예방센터(CDC)의 한타바이러스 기술 정보 인덱스 페이지]
- [[7](http://www.expasy.org/viralzone/all_by_species/213.html) Viralzone: Hantavirus]
- [[8](https://www.viprbrc.org/brc/home.spg?decorator=hanta) 바이러스 병원체 데이터베이스 및 분석 리소스(ViPR): Hantaviridae]